Banyak sekolah di Indonesia, salah satu topik praktikum pada pelajaran biologi mengenai enzim katalase. Para siswa biasanya setelah praktikum diminta untuk membuat sebuah laporan baik individu maupun kelompok. Berikut ini contoh laporan praktikum mengenai faktor-faktor yang memengaruhi enzim katalase yang bisa dijadikan bahan belajar untuk Anda. Selamat membaca!
BAB
I
PENDAHULUAN
1.1 Latar Belakang
Metabolisme merupakan suatu reaksi kimia yang terjadi di dalam tubuh makhluk hidup. Reaksi metabolisme tersebut dimaksudkan untuk memperoleh energi, menyimpan energi, menyusun bahan makanan, merombak bahan makanan, memasukkan atau mengeluarkan zat-zat, melakukan gerakan, menyusun struktur sel, merombak struktur-struktur sel yang tidak dapat digunakan lagi, dan menanggapi rangsang. Tentunya dalam suatu reaksi terdapat zat-zat atau senyawa-senyawa baik yang sifatnya menghambat (inhibitor) atau mempercepat reaksi (aktivator). Senyawa-senyawa yang mempercepat suatu reaksi dikenal dengan sebutan katalisator. Katalisator adalah suatu zat yang mempercepat laju reaksi kimia pada suhu tertentu, tanpa mengalami perubahan atau terpakai oleh reaksi tersebut. Suatu katalis berperan dalam reaksi tapi bukan sebagai pereaksi ataupun produk. Katalis memungkinkan reaksi berlangsung lebih cepat atau memungkinkan reaksi pada suhu lebih rendah akibat perubahan yang dipicunya terhadap pereaksi. Katalis menyediakan suatu jalur pilihan dengan energi aktivasi yang lebih rendah. Katalis mengurangi energi yang dibutuhkan untuk berlangsungnya reaksi.
Metabolisme yang merupakan reaksi kimia memiliki katalisator yang disebut dengan enzim. Enzim yang tersusun atas protein dan molekul lainnya bekerja dengan menurunkan energi aktivasi, sehingga tidak diperlukan suhu dan energi tinggi untuk melakukan suatu reaksi kimia di dalam tubuh. Jika tidak terdapat katalisator dalam metabolisme, maka suhu tubuh akan meningkat dan membahayakan bagi tubuh makhluk hidup. Kerja enzim tentunya dipengaruhi oleh faktor dalam dan luar enzim. Faktor dalam misalnya substansi – substansi genetik yang dibawa oleh masing – masing enzim.
Keinginan kami untuk mengetahui faktor luar yang memengaruhi kerja enzim merupakan suatu motivasi kami untuk melakukan percobaan sederhana yang menggunakan enzim katalase sebagai sampel.
Baca juga:
1.2 Rumusan Masalah
- Bagaimana cara kerja enzim katalase?
- Apakah pengaruh suhu tinggi terhadap kinerja enzim katalase?
- Apakah pengaruh suhu rendah terhadap kinerja enzim katalase?
- Apakah pengaruh pH asam terhadap kinerja enzim katalase?
- Apakah pengaruh pH basa terhadap kinerja enzim katalase?
1.3 Batasan Masalah
Kami hanya membahas dan menganalisis hasil percobaan yang telah kami lakukan yaitu mengetahui faktor yang memengaruhi enzim katalase dengan melakukan uji suhu dan pH.
1.4 Tujuan Penelitian
Kami hanya membahas dan menganalisis hasil percobaan yang telah kami lakukan yaitu mengetahui faktor yang memengaruhi enzim katalase dengan melakukan uji suhu dan pH.
- Mengetahui cara kerja enzim katalase.
- Mengetahui pengaruh suhu terhadap kinerja enzim katalase.
- Mengetahui pengaruh pH terhadap kinerja enzim katalase.
1.5 Manfaat Penelitian
- Untuk mengetahui cara kerja enzim katalase pada ekstrak hati ayam.
- Mengetahui pengaruh pH dan suhu terhadap enzim pada ekstrak hati ayam
BAB II
TINJAUAN
PUSTAKA
2.1 Kajian Teori
2.1.1 Pengertian Enzim
Menurut Syamsuri metabolisme sangat bergantung pada enzim. Enzim berperan sebagai pemercepat reaksi metabolisme di dalam tubuh makhluk hidup, tetapi enzim tidak ikut bereaksi.
2.1.2 Struktur Enzim.
Enzim merupakan protein yang tersusun atas asam – asam amino. Kebanyakan enzim berukuran lebih besar dari substratnya.akan tetapi,hanya daerah tertentu dari molekul enzim tersebut yang berikatan dengan substrat, yaitu bagian yang disebut dengan sisi aktif. Secara kimia, enzim yang lengkap (holoenzim) tersusun atas dua bagian, yaitu bagian protein dan bagian bukan protein.
- Bagian protein disebut apoenzim, tersusun atas asam – asam amino. Bagian protein bersifat labil (mudah berubah), misalnya terpengaruh oleh suhu dan keasaman.
- Bagian bukan protein yang disebut gugus protetik, yaitu gugusan yang aktif. Gugus prostetik yang berasal dari molekul non organik disebut kofaktor, misalnya besi, tembaga, zink. Gugus prostetik yang terdiri dari senyawa – senyawa kompleks disebut konenzim, misalnya NADH, FADH, koenzim A, tiamin, riboflavin, asam pantotenat, niasin, piridoksin, biotin, asam folat, dan kobalamin.
2.1.3 Ciri – Ciri Enzim
- Biokatalisator: enzim hanya dihasilkan oleh sel-sel mahkluk hidup yang digunakan untuk mempercepat proses reaksi.
- Protein: sifat-sifat enzim sama dengan protein yaitu dapat rusak pada suhu yang tinggi dan dipengaruhi PH.
- Bekerja Secara Khusus: enzim tertentu hanya dapat mempengaruhi reaksi tertentu, tidak dapat mempengaruhi reaksi lainnya. Zat yang terpengaruhi oleh enzim tersebut disebut substrat. Substrat adalah zat yang bereaksi. Oleh karena macam zat yang bereaksi di dalam sel sangat banyak, maka macam enzim pun banyak.
- Dapat Digunakan Berulang Kali: dapat digunakan berulang kali karena enzim tidak berubah pada saat terjadi reaksi. Satu molekul enzim dapat bekerja berkali-kali selama enzim itu tidak rusak.
- Rusak Oleh Panas: enzim rusak oleh panas karena merupakan suatu protein. Rusaknya enzim oleh panas disebut denaturasi, jika telah rusak enzim tidak dapat bekerja lagi.
- Tidak Ikut Bereaksi: enzim hanya diperlukan untuk mempercepat reaksi namun tidak ikut bereaksi.
- Bekerja Dapat Balik: suatu enzim dapat bekerja menguraikan suatu senyawa menjadi senyawa-senyawa lain dan sebaliknya dapat pula bekerja menyusun senyawa-senyawa itu menjadi senyawa semula.
- Kerja Enzim Dipengaruhi Faktor Lingkungan
2.1.4 Cara Kerja Enzim
- Teori Gembok - Anak Kunci
- Teori Induced Fit
2.1.5 Enzim Katalase
Enzim Katalase adalah enzim yang berperan dalam penguraian H2O2 (Hidrogen Peroksida) yang apabila tidak diurai akan menjadi senyawa beracun. Enzim ini terdiri atas 4 gugusan heme. Enzim ini ada pada tulang, ginjal, membran mukosa dan hati. Adapun aktifitas enzim katalase ini ditemukan di wilayah mitokondria, peroksosom dan juga sutoplasma. Enzim katalase ini mempunyai 4 rantai polupeptida yang pada masing-masing rantainya tersusun atas ± 500 asam amino. Selain itu, enzim katalase ini juga mempunyai empat kelompok heme yang terbetuk dari cincin protoporphyrin. Cincin ini mengandung atom besi yang tunggal. Adapun berat molekul tersebut sekitar 118.054,25 gram/mol.
Enzim katalase dimasukkan ke dalam golongan enzim hidroperoksidase di mana ia melindungi tubuh organisme dari senyawa peroksida yang berbahaya. Penumpukan senyawa iini bisa memancing radikal bebas yang jika tidak segera diuraikan akan membuat membran sel di dalam tubuh rusak dan memancing penyakit semacam kanker dan juga arterosklerosis.
Terjadinya reaksi antara H2O2 dibantu enzim katalase menjadi oksigen dan air ditandai dengan adanya gelembung dan menyala apabila dibakar. Ada tidaknya gelembung sebagai indikasi adanya air dalam wujud uap. Sedangkan menyala atau tidaknya bara merupakan indikator adanya gas oksigen dalam tabung tersebut.
Enzim katalase yang dihasilkan peroksisom pada hati akan mengalami denaturasi (kerusakan) pada suhu tinggi ataupun suasana asam dan basa. Enzim katalase bekerja secara optimal pada suhu kamar (±30° C) dan suasana netral.
2.1.6 H2O2 (Hidrogen Peroksida)
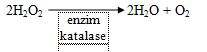
Hidrogen Peroksida atau H2O2 merupakan hasil pernapasan dan terdapat di dalam sel-sel organisme. H2O2 ditemukan oleh Louis Jacquea Thernard pada tahun 1818. Senyawa ini merupakan bahan kimia organik yang memiliki sifat oksidator kuat dan bersifat racun bagi tubuh. H2O2 ini harus segera diubah menjadi bentuk yang lebih tidak berbahaya (O2 dan H2O). Bentuk reaksi kimianya adalah:

2.2 Hipotesis
Berdasarkan kajian teori diatas, dapat ditarik hipotesis sebagai berikut:
 Suhu (75°C, 0,8°C dan suhu ruangan )
Suhu (75°C, 0,8°C dan suhu ruangan )
 pH sistem (diberi NaOH, HCl, dan netral)
pH sistem (diberi NaOH, HCl, dan netral)
 Volume ekstrak hati ayam
Volume ekstrak hati ayam
 Volume H2O2
Volume H2O2
 Jumlah gelembung yang dihasilkan
Jumlah gelembung yang dihasilkan
 Perubahan warna sample
Perubahan warna sample
 Nyala bara api
Nyala bara api
Hidrogen Peroksida atau H2O2 merupakan hasil pernapasan dan terdapat di dalam sel-sel organisme. H2O2 ditemukan oleh Louis Jacquea Thernard pada tahun 1818. Senyawa ini merupakan bahan kimia organik yang memiliki sifat oksidator kuat dan bersifat racun bagi tubuh. H2O2 ini harus segera diubah menjadi bentuk yang lebih tidak berbahaya (O2 dan H2O). Bentuk reaksi kimianya adalah:

2.2 Hipotesis
Berdasarkan kajian teori diatas, dapat ditarik hipotesis sebagai berikut:
- Kerja enzim akan sangat dipengaruhi oleh suhu dan derajat keasaman lingkungannya.
- Enzim katalase akan bekerja lebih optimal pada suhu kamar ± 30°.
- Enzim katalase akan bekerja lebih optimal pada pH netral (6,5-7,5).
BAB III
METODE
PENELITIAN
3.1 Variabel Penelitian
a. Variabel bebas
b. Variable kontrol
c. Variable terikat
3.2 Definisi Operasional
a. Definisi Operasional Variabel Manipulasi (Bebas)
3.3 Rancangan Penelitian
Sample A: Perlakuan tanpa perubahan suhu maupun pH
Sample B: Perlakuan dengan diberi HCl 4 tetes
Sample C: Perlakuan dengan diberi NaOH 4 tetes
Sample D: Perlakuan dengan direndam pada suhu 5°C
Sample E: Perlakuan dengan direndam pada suhu 0,8°C
3.4 Sasaran Penelitian
Populasi : Hati ayam
Sample : Ekstrak hati ayam
3.5 Alat dan Bahan
 Tabung Reaksi 6 buah
Tabung Reaksi 6 buah
 Gelas Beaker 3 buah
Gelas Beaker 3 buah
 Rak Tabung Reaksi 1 buah
Rak Tabung Reaksi 1 buah
 Pembakar Spirtus 1 buah
Pembakar Spirtus 1 buah
 Termometer 1 buah
Termometer 1 buah
 Mortar 1 buah
Mortar 1 buah
 Pipet 3 buah
Pipet 3 buah
 Korek Api 1 buah
Korek Api 1 buah
 Lidi 1 buah
Lidi 1 buah
 Hati Ayam 1 buah
Hati Ayam 1 buah
 HCl 4 tetes
HCl 4 tetes
 NaOH 4 tetes
NaOH 4 tetes
 H2O2 10% 6 tetes
H2O2 10% 6 tetes
 Es batu secukupnya
Es batu secukupnya
 Air secukupnya
Air secukupnya
3.6 Langkah-Langkah Kerja Penelitian
3.8 Cara (Rencana) Analisis Data
- Sample A tidak diberi perlakuan
- Tingkat pH yang diberlakukan pada ekstrak hati yang berbeda pada 2 dari 6 sample (Sample B dan C).
- Suhu yang diberlakukan pada ekstrak hati ayam yang berbeda pada 2 dari 6 sample (Sample D dan E).
- Jumlah gelembung yang dihasilkan berdasarkan pengamatan mata.
- Perubahan warna sample dari warna setelah diberi perlakuan menjadi warna endapan setelah diberi H2O2
- Terangnya Nyala api ketika dimasukkan dalam tabung reaksi.
Sample A: Perlakuan tanpa perubahan suhu maupun pH
Sample B: Perlakuan dengan diberi HCl 4 tetes
Sample C: Perlakuan dengan diberi NaOH 4 tetes
Sample D: Perlakuan dengan direndam pada suhu 5°C
Sample E: Perlakuan dengan direndam pada suhu 0,8°C
3.4 Sasaran Penelitian
Populasi : Hati ayam
Sample : Ekstrak hati ayam
3.5 Alat dan Bahan
Alat:
Bahan:
3.6 Langkah-Langkah Kerja Penelitian
- Membuat ekstrak ayam dengan cara menumbuknya dan disaring.
- Mengisi 5 tabung reaksi dengan ekstrak hati ayam kemudian melabel tabung reaksi dengan huruf A, B, C, D, dan E.
- Meneteskan 4 tetes HCl ke tabung reaksi B.
- Meneteskan 4 tetes NaOH ke tabung reaksi C.
- Merendam tabung reaksi D ke dalam air bersuhu 75° C.
- Merendam tabung reaksi E ke dalam air bersuhu 0,8° C.
- Meneteskan H2O2 ke masing-masing tabung kemudian memasukkan bara lidi ke masing tabung reaksi.
- Mengamati perubahan yang terjadi lalu mencatat hasilnya.
3.8 Cara (Rencana) Analisis Data
Membandingkan hasil antara satu perlakuan dengan perlakuan yang lain.
BAB IV
HASIL DAN
PEMBAHASAN
4.1 Hasil Penelitian
Jika tabel terpotong, silahkan rotasi layar HP
No
|
Perlakuan
|
Kecepatan reaksi
|
Hasil
|
1
|
Sample A
(tanpa perlakuan)
|
+++
|
Jumlah gelembung :banyak
|
Perubahan warna :tetap
coklat muda
|
|||
Nyala api :terang
|
|||
2
|
Sample B
(ditambahkan HCl)
|
+
|
Jumlah
gelembung :sangat
sedikit
|
Perubahan
warna :tetap coklat tua
|
|||
Nyala api :redup
|
|||
3
|
Sample C
(ditambahkan NaOH)
|
++
|
Jumlah
gelembung :sedikit
|
Perubahan
warna :coklat muda menjadi lapisan bawa coklat merah dan atas coklat kuning
|
|||
Nyala api :sedikit
terang
|
|||
4
|
Sample D (suhu 75° C)
|
-
|
Jumlah
gelembung :tidak ada
|
Perubahan warna :tetap
coklat sangat muda (terjadi pengendapan)
|
|||
Nyala api :tidak
menyala
|
|||
5
|
Sample E (suhu 0,8° C)
|
+++
|
Jumlah
gelembung :banyak
|
Perubahan warna :tetap
coklat muda
|
|||
Nyala api :terang
|
+++ = reaksi paling cepat
++ = reaksi sedikit cepat
+ = reaksi lambat
̶ = tidak ada reaksi
Perubahan warna dilihat dari setelah diperlakukan sampai setelah ditetesi H2O2
4.2 Pembahasan
Berdasarkan praktikum yang telah kami lakukan, kami menggunakan 2 macam uji pengaruh enzim katalase berdasarkan faktor yang mempengaruhi, yaitu:
1. Suhu
Untuk mengetahui pengaruh suhu terhadap enzim, sample diuji dengan merendamnya pada air dengan suhu tertentu. Di sini, kami menggunakan suhu 75°C dan 0,8°C
2. pH
Untuk mengetahui pengaruh pH terhadap enzim, sample diuji dengan meneteskan sejumlah larutan yang memiliki sifat asam (HCl) dan basa (NaOH).
Kemudian setiap sample diteteskan sejumlah larutan H2O2 10%. Jika setelah diteteskan H2O2 terbentuk gelembung, menandakan bahwa terjadi reaksi pemecahan H2O2 menjadi H2O dan O2. Gelembung tersebut merupakan tanda adanya kandungan air dalam wujud uap. Setelah itu dimasukkan bara api untuk membuktikan adanya O2 atau tidak. Apabila api tetap hidup berarti ada gas O2 di dalam tabung reaksi. Berikut ini merupakan uraian dari hasil praktikum kami:
- Sample A (tanpa perlakuan)
- Sample B (ditetesi HCl)
- Sample C (ditetesi NaOH)
- Sample D (suhu 75°C)
- Sample E (suhu 0,8°C)
BAB V
PENUTUP
5.1 Kesimpulan
Dari praktikum yang telah dilakukan dapat disimpulkan bahwa:
Dari praktikum yang telah dilakukan dapat disimpulkan bahwa:
- Enzim katalase adalah enzim yang membantu proses penguraian H2O2 yang bersifat racun menjadi air (H2O) dan oksigen (O2) tanpa ikut bereaksi bersama. Berikut reaksi pemecahan H2O2 :

- Enzim katalase terdapat di hati, praktikum ini membuktikan bahwa fungsi hati sebagai tempat penetralisir racun.
- Kerja enzim katalase dipengaruhi oleh suhu dan pH.
- Enzim katalase tidak dapat bekerja pada suhu yang terlalu panas namun pada suhu dingin enzim dapat bekerja optimal. Berarti enzim katalase bekerja dengan optimal tidak hanya pada suhu kamar ± 30° (tanpa perlakuan) saja namun pada suhu dingin juga bekerja.
- Kerja Enzim katalase juga dipengaruhi oleh pH. Apabila lingkungannya asam atau basa enzim katalase tetap bisa bekerja namun kurang optimal. Enzim katalase bekerja pada pH 6,5-7,5.
- Adanya gelembung dalam reaksi menandakan adanya uap air dan bara api menyala menandakan adanya gas O2 (pembuktian hasil dari pemecahan H2O2).
- Terjadi beberapa kesalahan dalam praktikum, yaitu takaran ekstrak hati yang digunakan tidak sama, ada jeda antara setelah penetasan H2O2 dengan pemasukkan bara api, dan penetesan H2O2 yang sedikit lama sehingga suhu bisa saja sudah berubah.
5.2 Saran
- Sebaiknya ekstrak hati yang digunakan takarannya disamakan agar hasil yang didapat lebih akurat.
- Sebaiknya penetesan H2O2 untuk sample dengan perlakuan suhu 75°C dan 0,8°C tidak terlalu lama agar suhunya tidak berubah.
- Sebaiknya saat memasukkan bara api secepat mungkin setelah diteteskan H2O2 agar hasil penentuan kecepatan reaksi lebih akurat.
BAB
VI
ANALISIS
DATA DAN JAWABAN
6.1 Pertanyaan/Analisis Data
- Tuliskan reaksi kimia yang terjadi!
- Bagaimana pengaruh enzim katalase terhadap H2O2?
6.2 Jawaban
- Reaksi kimia yang berlangsung pada enzim katalase adalah sebagai berikut:
- Pengaruh enzim katalase terhadap H2O2, yaitu enzim katalase akan menguraikan H2O2 menjadi uap air dan oksigen. Enzim katalase dapat menguraikan H2O2 dengan baik apabila kondisi lingkungan bersuhu ±30°C dan pH lingkungan sekitar 6,5-7,5.atau netral.

Terima kasih telah berkunjung ke blog saya. Jika ada koreksi ataupun saran, silahkan tinggalkan komentar di kolom komentar.
EmoticonEmoticon